zzgl. MwSt.
- Virtual Classroom-Preis: 996,55 € zzgl. MwSt.
- Dauer: 2 Tage (von 09:00 - 17:00 Uhr)
- Servicebausteine: im Wert von 249.80 €
- Artikelnummer: L220
- Max. Teilnehmer: 15
- Kursform: Präsenz oder Virtual Classroom
- Seminarinfo: PDF-Download
- Inhouse: Ihre unverbindliche Anfrage
-
Nächste Termine:
Düsseldorf NH Hotel City Nord - 03.06. - 04.06.25. Oliver Kirn
![Jetzt diesen Termin buchen!]()
Live Virtual-Classroom-Training - 03.06. - 04.06.25. Oliver Kirn
![Jetzt diesen Termin buchen!]()
Berlin NH Hotel City Ost - 19.08. - 20.08.25. Sven Beerheide
![Jetzt diesen Termin buchen!]()
Frankfurt Mercure Hotel und Residenz Messe - 07.10. - 08.10.25. Bernd Stadter
![Jetzt diesen Termin buchen!]()
Live Virtual-Classroom-Training - 07.10. - 08.10.25. Bernd Stadter
![Jetzt diesen Termin buchen!]()
Live Virtual-Classroom-Training - 26.11. - 27.11.25. Bernd Stadter
![Jetzt diesen Termin buchen!]()
Ludwigsburg nestor Hotel - 26.11. - 27.11.25. Bernd Stadter
![Jetzt diesen Termin buchen!]()
Alle Termine anzeigen
-
-
Weitere Kursformate:
Das Qualitätsmanagement Medizinprodukte Basiswissen Seminar vermittelt Ihnen einen idealen Einstieg in das QM-System nach ISO 13485. Dabei lernen Sie die Norm DIN EN ISO 13485 und deren Anforderungen von Grund auf kennen und erfahren alles über die erfolgreiche Betreuung und falls noch nicht geschehen Einführung und Zertifizierung eines QM-Systems für Medizinprodukte. Die ISO 13485 dient im Bereich der Medizinprodukte ebenfalls zur Erfüllung gesetzlicher Forderungen.
In der Schulung lernen Sie die Gliederung, den Inhalt, die Anwendungsbereiche sowie Ausschlüsse der Norm ISO 13485 für Medizinproduktehersteller genau kennen. Sie erwerben zudem alle Kompetenzen, um das QM-System erfolgreich dauerhaft zu betreuen und alle damit verbundenen Aufgaben normkonform umzusetzen. Wir bieten Ihnen somit in nur zwei Tagen Intensivtraining einen idealen Einstieg in die ISO 13485 - egal ob Sie vor dem Aufbau eines Qualitätsmanagement Systems für Medizinprodukte stehen oder mit vorhandenen Strukturen in Ihrem Unternehmen arbeiten. Mit diesem Basiswissen Seminar zum Qualitätsmanagement für Medizinprodukte können Sie dieser Aufgabe gelassen entgegentreten. Ihre Trainer in diesem ISO 13485 Seminar verfügen über jahrelange Erfahrung beim Aufbau und der Einführung von Qualitätsmanagementsystemen nach ISO 13485 und können so aus einem breiten Erkenntnisschatz schöpfen, um Ihre individuellen Fragen in der Ausbildung zu beantworten und Ihnen praktische Hilfestellung zu leisten!
Nach Ihrer Präsenzphase erhalten Sie Zugang zum E-Learning Kurs "Praxistransfer / Praxistipps & Methoden", welcher noch einmal alle wichtigen Themen aufgreift, inhaltlich weiter vertieft und durch die Praxisnähe noch mehr Verständnis zu allen Forderungen generiert sowie geeignete Methoden vorstellt.

Kostenlos für Sie: Prozessbeschreibung Vorlage kostenlos - Prozessbeschreibung erstellen - Erfinden Sie das Rad nicht neu! Die Nutzung beinhaltet keine Folgeverpflichtungen, kein Abo und bedarf keiner Kündigung in irgendeiner Form! Details >
Was sind die Inhalte Ihres Basiswissen Seminars zum Qualitätsmanagement für Medizinprodukte?
In diesem Basiswissen Seminar zum Qualitätsmanagement für Medizinprodukte lernen Sie die Norm ISO 13485 und ihre Forderungen detailliert kennen. Sie erfahren dabei, wie Sie ein QM-System für Medizinprodukte umsetzen und dauerhaft betreuen. Ihr Trainer gibt Ihnen dabei zahlreiche hilfreiche Expertentipps mit auf den Weg und beantwortet auch alle Ihre individuellen Fragen.
Einführung in das Qualitätsmanagement für Medizinprodukte
Ihre Ausbildung beginnt mit einer kurzen Einführen in den Themenbereich Qualitätsmanagement für Medizinprodukte. Dabei werden wichtige Begriffe definiert und es wird ein kurzer Blick auf die historische Entwicklung geworfen.
- Was ist Qualität?
- Definition Medizinprodukte
- Qualitätsmanagement für Medizinprodukte
- Entwicklung des Qualitätsmanagements für Medizinprodukte
Anforderungen des Medizinprodukterechtdurchführungsgesetzes MPDG und der europäischen Verordnungen MDR & IVDR
Im Medizinproduktebereich sind gesetzliche Vorgaben auf nationaler und europäischer Ebene von immens großer Bedeutung, um die Sicherheit des Endverbrauchers zu gewährleisten. Dieses Basiswissen Seminar zum Qualitätsmanagement für Medizinprodukte widmet sich ausführlich den gesetzlichen Anforderungen des MPDG, der MDR sowie IVDR.
- Medizinprodukterechtdurchführungsgesetzes MPDG
- EU Verordnung für Medizinprodukte MDR (Medical Device Regulation)
- EU Verordnung für In-vitro-Diagnostika IVDR (In-vitro Diagnostics Regulation)
- Herstellerpflichten
- Praxisübungen: Klassifizierung eines Medizinproduktes
Die Norm DIN EN ISO 13485:2021
Ihr Trainer erläutert Ihnen in diesem Kurs zunächst Grundlagen sowie den Anwendungsbereich der ISO 13485 für Ihr Qualitätsmanagementsystem im Bereich Medizinprodukte.
- Entstehung
- Anwendungsbereich
- Unterschiede zwischen den Normen DIN EN ISO 9001 und DIN EN ISO 13485
Welche Anforderungen stellt die ISO 13485 im Detail?
Die letzte, größte thematische Einheit dieses Basiswissen Seminars zum Qualitätsmanagement für Medizinprodukte befasst sich dann ausführlich mit der Norm. Sie werden Schritt für Schritt durch die Norm geführt und lernen alle Anforderungen der DIN EN ISO 13485:2021 an Ihr Qualitätsmanagementsystem kennen.
- Begriffe und Definitionen
- Allgemeine Anforderungen an ein Qualitätsmanagementsystem
- QSVs und Anforderungen an die Dokumentation
- Verantwortung der Leitung
- Managementbewertung
- Verantwortung, Befugnisse und Kommunikation
- Management von Ressourcen, Schulung
- Planung der Produktrealisierung, Entwicklung
- Gebrauchstauglichkeit von Medizinprodukten
- Praxistransfer: Entwicklung von Produkten oder Prozessen
- Validierung und Verifikation
- Schnittstellen zum Risikomanagement
- Risikomanagement nach ISO 14971
- Beschaffung: Zulieferer und ausgegliederte Prozesse
- Praxistransfer zum Lieferantenmanagement
- Produktion sowie Dienstleistungserbringung
- Messung, Analyse und Verbesserung
Welches Zertifikat und welche Qualifikationsbescheinigung erhalten Sie nach diesem ISO 13485 Basiswissen Seminar?
Sie erhalten eine Qualifikationsbescheinigung zur Teilnahme an dem Basiswissen Seminar zum Qualitätsmanagement für Medizinprodukte in Deutsch sowie in Englisch. Die englische Qualifikationsbescheinigung ist dabei als Serviceleistung im Preis enthalten. Die Qualifikationsbescheinigung dokumentiert dabei die behandelten Inhalte sowie die Schulungsdauer und dient Ihnen als Nachweis Ihrer Teilnahme an der Schulung.


Was ist das Ziel dieses Basiswissen Seminars zum...
Welche Zielgruppe sprechen wir mit diesem Kurs an?Dabei...
Voraussetzungen für die Teilnahme an dieser ISO 13485...
Was ist das Ziel dieses Basiswissen Seminars zum Qualitätsmanagement für Medizinprodukte?
Ziel dieses Basiswissen Seminars zum Qualitätsmanagement für Medizinprodukte ist es, Sie umfassend in die ISO 13485 einzuführen. Sie werden dabei in die Lage versetz, die Anforderungen der DIN EN ISO 13485 im Qualitätsmanagementsystem umzusetzen und dieses dauerhaft zu betreuen und weiterzuentwickeln. Somit sind Sie für künftige Aufgaben im QM von Medizinprodukten gewappnet und können im QM-Team bei Medizinpodukteherstellern mitwirken.
Welche Zielgruppe sprechen wir mit diesem Kurs an?
Dabei eignet sich die Schulung für Qualitätsmanagementbeauftragte, die Unternehmensleitung und sonstiges Fachpersonal im QM-Bereich, welches im Unternehmen für den Bereich des QM-Systems zuständig ist. Aber auch Händler, Hersteller und Importeure von Medizinprodukten aus den Bereichen Zulassung, Regulatory Affairs, Qualitätsmanagement sowie Dienstleister aus der Medizinproduktbranche, die ein QM-System nach DIN EN ISO 13485 einführen oder dauerhaft betreuen wollen gehören zur Zielgruppe dieser Schulung.
Voraussetzungen für die Teilnahme an dieser ISO 13485 Schulung
Es sind keine speziellen Voraussetzungen zur Teilnahme an dem ISO 13485 Seminar "Basiswissen QM Medinzinprodukte" erforderlich.
Ihre Servicebausteine in diesem Qualitätsmanagement Medizinprodukte Basiswissen - ISO 13485 Seminar Kurs:
Als Kursteilnehmer erhalten Sie folgende Servicebausteine im Rahmen Ihrer Kursteilnahme. Diese Bausteine sind im Seminarpreis bereits enthalten und unterstützen Sie mit zusätzlichen Inhalten und Musterdokumenten zu Ihrem Kursthema. Den monatlichen Expertenbrief erhalten Sie erstmalig im Anschluss an Ihre Teilnahme. Dieser informiert Sie monatlich über aktuelle Fachinfos zu Ihrem Kursthema.
| E-Kurs: | Praxistransfer / Praxistipps und Methoden zur Schulung Basiswissen EN ISO 13485 - Qualitätsmanagement für Medizinprodukte Hersteller Im Wert von 149,90 € |
|
| Vorlagen: | Basispaket Prozesse und Systeme Im Wert von 99,90 € |
|
| Fachinfo: | Ihr monatlicher Expertenbrief Exklusive Expertentipps und Fachwissen für Sie |
Weitere mögliche Schritte Ihrer Ausbildung
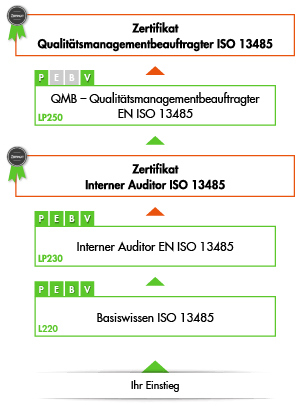
Das Basiswissen Seminar zum Qualitätsmanagement für Medizinprodukte ist Teil des modularen Ausbildungsprogramms der VOREST AG im Bereich der ISO 13485. Sie ist der erste von drei Ausbildungsschritten hin zur Prüfung zum international anerkannten QMB ISO 13485. Jede Schulung kann aber selbstverständlich auch unabhängig von der Gesamtausbildung einzeln besucht werden.
1. Schritt: Basiswissen Qualitätsmanagement Medizinprodukte DIN EN ISO 13485
2. Schritt: Interner Auditor DIN EN ISO 13485
3. Schritt: Qualitätsmanagementbeauftragter ISO 13485 - QMB Medizinprodukte
Alle Schulungen und Qualifizierungsabschlüsse der VOREST AG sind national und international anerkannt. Die VOREST AG ist akkreditierter Personalzertifizierer, was Ihnen die Sicherheit gibt, eine wertvolle Ausbildung zu erhalten.
|
Seite 0 von 0
|